La Administración de Alimentos y Medicamentos de Estados Unidos (FDA) autorizó mediante la vía 510(k) la comercialización de Encora X1™, un dispositivo portátil de neuroestimulación diseñado para aliviar el temblor de la mano en adultos con temblor esencial. Esta condición neurológica progresiva afecta a más de siete millones de personas en Estados Unidos y puede interferir significativamente con actividades cotidianas como escribir, comer o abotonarse una camisa.
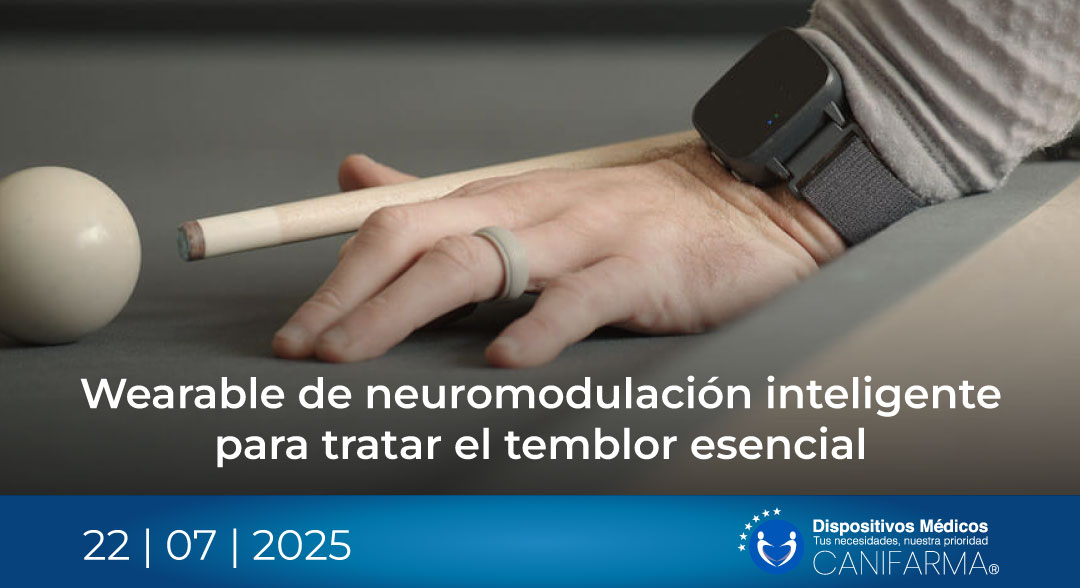
Encora X1 es un dispositivo de prescripción que se lleva en la muñeca, con un formato similar al de un reloj inteligente. Su funcionamiento se basa en algoritmos que detectan en tiempo real el patrón rítmico del temblor y aplican una estimulación eléctrica personalizada en el nervio periférico de la muñeca. Esta estimulación busca modular las señales neuronales responsables del temblor, reduciendo su amplitud mientras el dispositivo está activo, sin recurrir a fármacos ni a procedimientos quirúrgicos.
La autorización se sustentó en los resultados de dos estudios clínicos: un ensayo aleatorizado con control simulado (sham) y un estudio de uso domiciliario de 90 días. En conjunto, los datos mostraron mejoras consistentes tanto en la severidad del temblor como en el desempeño de tareas funcionales, incluyendo actividades como beber de un vaso o escribir. Según los investigadores, estos resultados son particularmente relevantes para pacientes que no responden adecuadamente a medicamentos o que no toleran sus efectos adversos.
El temblor esencial suele tratarse inicialmente con terapia farmacológica, pero aproximadamente la mitad de los pacientes experimenta eficacia limitada o efectos secundarios significativos. En casos refractarios, las opciones pueden incluir intervenciones invasivas como estimulación cerebral profunda. En este contexto, dispositivos de neuromodulación no invasiva como Encora X1 representan una alternativa intermedia que puede ofrecer alivio sintomático sin los riesgos asociados a la cirugía.
En términos de seguridad, los eventos adversos reportados en los ensayos fueron en su mayoría leves y transitorios, incluyendo irritación cutánea, sensación de hormigueo o debilidad temporal en la extremidad tratada. El dispositivo no constituye una cura para el temblor esencial, sino una herramienta de manejo sintomático durante su uso. Tras la autorización regulatoria, la compañía prevé un despliegue gradual en Estados Unidos, mientras avanza en acuerdos de reembolso y distribución para facilitar el acceso a esta tecnología de neuromodulación portátil.